Nicht-muskelinvasives Blasenkarzinom
A Study of Erdafitinib Versus Investigator Choice of Intravesical Chemo-therapy in Participants Who Received Bacillus Calmette-Guérin (BCG) and Recurred With High Risk Non-Muscle-Invasive Bladder Cancer (THOR2)
Welche Patientengruppe wird in die Studie eingeschlossen?
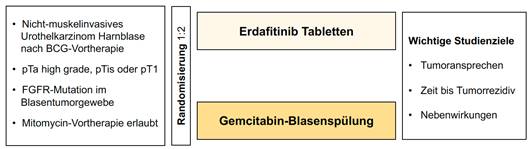
Patienten mit einem oberflächlichen Hochrisiko-Urothelkarzinom der Harnblase mit den Tumorstadien pTa high grade, pTis oder pT1, die auf eine BCG-Blasenspülung nicht angesprochen haben. Zusätzlich liegt eine spezielle Änderung der Erbinformation (Mutation Fibroblasten-Wachstumsrezeptor FGFR) im Blasentumor-gewebe vor.
Welche Vortherapien sind erlaubt?
- BCG-Blasenspülungen
- Mitomycin-Blasenspülungen
Welche Vortherapien sind nicht erlaubt?
- Vorbehandlung mit einem FGFR-Inhibitor
Gibt es Ausschlusskriterien für die Studie?
- Zweittumor in den letzten 2 Jahren
- Erkrankungen der Netzhaut
- Schwere Herz-Kreislauf-Erkrankung
Wie funktioniert die Phase-II Studie?
Vor Einschluss in die Studie muss zunächst das bereits vorhandene Blasentumorgewebe auf das Vorliegen einer Mutation des Fibroblasten-Wachstumsrezeptors (FGFR) untersucht werden. Falls die FGFR-Mutation vorliegt, werden die Patienten nach dem Zufallsprinzip in zwei Gruppen aufgeteilt:
Die Kontrollgruppe erhält Blasenspülungen mit den Chemotherapeutikum Gemcitabin, zunächst im Wochenrhythmus, später im Monatsrhythmus. Die Studiengruppe erhält den FGFR-Inhibitor Erdafitinib in Tablettenform. Die Studie ist nicht verblindet. Arzt und Patient wissen, welche Therapie verabreicht wird.
Was für eine neue Tumortherapie wird untersucht?
Untersucht wird die Therapie mit dem Medikament Erdafitinib in Tablettenform. Erdafitinib ist ein FGFR-Inhibitor und blockiert speziell den Stoffwechselweg der Tumorzelle, so dass die Tumorzellaktivität ausgebremst wird.
Wie ist die Studie aufgebaut?
Wo finde ich ausführliche Informationen:
www.clinicaltrials.gov NCT04172675
